NeuroImage新发:想要静下来没那么容易!研究揭示“降低心率”比“加快心率”更消耗脑力
研究背景
大脑与心脏之间的双向通信是维持人体生理稳态和适应环境需求的核心机制。传统观点认为这种交流主要是“自上而下”的——即大脑通过自主神经系统调控心脏活动。然而,越来越多的证据表明,心脏活动也会通过迷走神经和脊髓传入通路向大脑传递内脏信号,影响情绪调节和内感受意识。这种脑心交互(Brain-Heart Interplay, BHI)的紊乱与抑郁、焦虑及认知功能下降密切相关。
尽管脑心关系在静息状态、情绪诱导等情境中已有广泛研究,但在主动自我调节情境下的动态机制仍属未知。生物反馈(Biofeedback)技术为探索这一“黑箱”提供了独特窗口——它允许个体通过实时生理信号反馈学习自主控制心脏活动。本研究首次将脑心交互指数(BHI)应用于心率生物反馈(HRBF)任务,旨在揭示主动调节心率过程中神经与心脏活动的双向耦合模式,为理解自我调控的生理机制开辟新前沿。

研究方法
本研究采用2×2被试内实验设计,45名健康大学生(62%女性,平均年龄23.27岁)在实验室完成单次心率生物反馈实验。
实验任务: 被试需在电脑屏幕前完成心率调节挑战。屏幕上会出现视觉提示符(向上箭头表示需加快心率,向下箭头表示需减慢心率)。有反馈条件:屏幕中央会显示一个随被试实时心率上下移动的蓝色圆环。只有当心率变化超过个体基线 ±2 bpm(成功阈值)时,圆环才会发生显著位移,作为直观的“生物反馈”。无反馈条件:屏幕仅显示方向箭头,不提供圆环位置变化。被试需完全依赖内感受(Interoception)来判断心率变化。每个试次持续2分钟,被试需尽可能长时间地让心率维持在目标范围内。
生理记录:使用32导联ANT Neuro放大器记录脑电图(EEG,采样率1000Hz),同时采集心电图(ECG)和呼吸信号(采样率256Hz)以控制混杂变量。
研究结果
重复测量ANOVA显示,调节方向(F(1,35) = 14.21, p < .001)和反馈条件(F(1,35) = 4.30, p = .005)均显著影响自我调节表现。具体而言,增加心率条件显著优于降低心率条件;有反馈条件显著优于无反馈条件。这一发现印证了经典观点:未经训练者往往更容易主动提高生理唤醒水平,而非降低它。
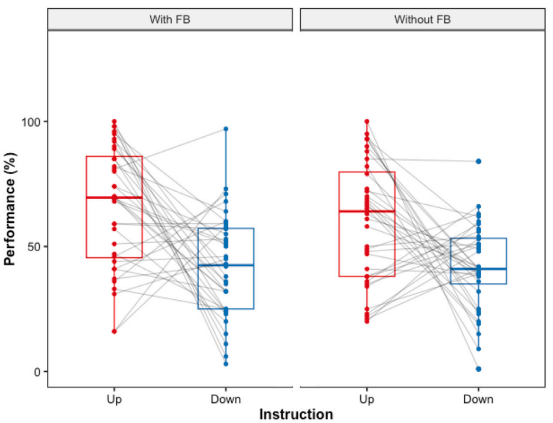
图1 自我调节任务表现箱线图
Wilcoxon检验揭示,无反馈条件下的脑→心BHI指数显著高于有反馈条件。具体表现为:无反馈时,EEG的θ、α、β频段向HRV高频段(HF)的信息传递更强。这表明当外部视觉反馈缺失时,被试需要动用更强的自上而下认知控制来调节心脏活动,可能涉及主动认知策略的调用。
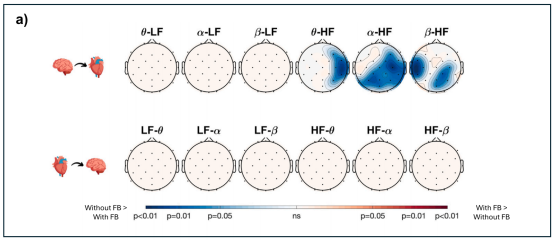
图2 有无反馈的BHI地形图
在降低心率条件下,脑→低频HRV(LF)的信息流显著强于增加心率条件。同时,降低心率时θ和β频段向HF的信息流也更高。这提示降低心率需要更显著的认知努力和自主神经调控,可能涉及前额叶抑制机制的参与和突显网络的激活,以协调交感和副交感神经的复杂互动。
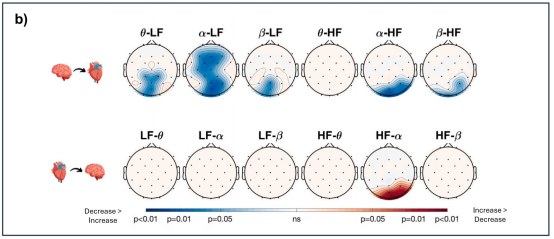
图3 增减心率方向的BHI地形图
相反,在增加心率条件下,HF→α的BHI指数显著更高。这一模式反映了心脏向大脑传递的迷走神经信号对皮层活动的自下而上调节,提示增加心率过程中大脑对迷走神经活性变化的监控更为敏感,确保自主调节的精确性。
此外,增加心率条件下的LF功率显著低于降低心率条件。值得注意的是,无论反馈是否存在,降低心率时LF和HF功率均更高,表明该条件诱发了更强烈的自主神经活动重组,趋向于一种由迷走神经主导的低唤醒状态。
结论和意义
本研究首次系统描绘了主动心率调节过程中的脑心动态交互图谱,揭示了三个核心机制:(1)增加心率更易实现,符合进化预设的应激反应模式;(2)降低心率需要更强的认知投入和自上而下控制,涉及更复杂的前额叶自主神经协调;(3)视觉反馈的存在减轻了认知负荷,使调节过程更依赖自下而上的反应性机制。
这些发现对神经反馈训练、焦虑抑郁干预及压力管理具有重要启示:临床实践中,针对心率降低的训练可能需要更长期的认知策略指导;而开发结合实时反馈与认知策略的个性化干预方案,有望优化自我调控效率。此外,研究采用的SDG模型为量化脑心双向通信提供了标准化工具,为未来探索情绪障碍、心血管疾病中的脑心解耦机制奠定了基础。
参考文献:Mura, F., Ruggiero, V., Catrambone, V., & Patron, E. (2026). Brain–heart interplay modulation during biofeedback: A new frontier in understanding selfregulation. NeuroImage, 326, 121695. https://doi.org/10.1016/j.neuroimage.2026.121695




