「以痛止痛」还是「火上浇油」?深圳大学彭微微团队揭示α-tACS调控疼痛预期与感知的神经机制
研究背景
疼痛感知并非单纯由感觉输入决定,而是深受大脑预期过程的影响。当个体预期疼痛即将发生时,对侧感觉运动皮层的α振荡(约8-12 Hz)会出现显著抑制,这一现象反映了感觉皮层为接收传入疼痛信号所做的“门控”准备。研究表明,感觉运动α振荡的强度与随后的疼痛敏感性呈负相关:振荡功率越高,个体报告的疼痛强度和神经反应通常越低。这一关联为神经调控策略提供了理论基础——增强疼痛预期阶段的α振荡,可能成为降低疼痛感知的潜在途径
经颅交流电刺激(tACS)作为一种无创神经调控技术,能够通过外源性振荡电流夹带并增强内源性脑节律。已有研究证实,α-tACS可有效提升大脑α振荡功率,且其效应具有一定的持续性。然而,疼痛预期的情境因素——尤其是预期的确定性程度——可能对这一调控效果产生重要影响。在不确定情境下,大脑的预期机制与确定性情境存在显著差异,表现为α振荡抑制减弱和疼痛处理模式的改变。因此,本研究旨在探讨感觉运动α-tACS对疼痛预期和感知的即时与持续影响,重点关注预期确定性如何塑造这些效应,并揭示其背后的神经振荡机制。

研究方法
研究采用双盲、假刺激对照的混合实验设计。共纳入80名健康右利手被试,随机分配至真刺激组(n=40)或假刺激组(n=40),最终有效样本为76人(每组38人)。所有被试分别在刺激前(T0)、刺激结束后立即(T1)及刺激结束后30分钟(T2)完成疼痛评估任务。
刺激方案采用高精度4×1环状电极布局,精准靶向右侧感觉运动皮层(以C4电极为中心)。真刺激组接受20分钟、10 Hz、1 mA峰峰值的α-tACS;假刺激组仅在刺激开始和结束各给予1分钟刺激,以模拟双盲条件。
疼痛评估任务包含两种视觉线索:确定性线索(红圈,100%出现疼痛刺激)和不确定性线索(红圈内白色问号,50%概率出现疼痛或无痛刺激)。采用Nd:YAP红外激光器诱发疼痛,作用于左手背侧,刺激强度经校准至中等疼痛水平(NRS=6)。EEG数据使用32通道ANT Neuro系统同步采集,采样率1000 Hz,离线处理包括1-30 Hz带通滤波、独立成分分析去伪迹及重参考至双侧乳突。
数据分析策略主要聚焦于两个关键时间窗口:
(1) 疼痛感知阶段(刺激后): 提取激光诱发脑电位(LEP)中标志性的N2和P2成分,以客观评估大脑对疼痛的神经反应强度。
(2) 疼痛预期阶段(刺激前): 分析疼痛来临前大脑的神经振荡节律,重点关注θ频段(4-8 Hz)和α频段(8-12 Hz)的功率变化,探究大脑在“等待疼痛”时的准备状态。
统计分析重点对比了刺激前后(即时与持续效应)、组别(真/假刺激)以及情境(预期确定/不确定)对上述脑电指标的影响。此外,研究还构建了中介效应模型,以揭示脑电振荡变化如何最终影响主观的疼痛评分。
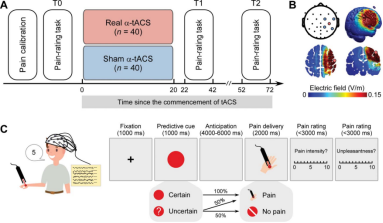
图1 研究设计与实验流程示意图
研究结果
1. 主观疼痛评分未见显著组间差异
行为学层面的分析显示,无论是在刺激结束后立即(T1)还是30分钟后(T2),也无论被试面临的是确定性还是不确定性的疼痛预期情境,接受真α-tACS干预与假刺激的被试在主观报告的疼痛强度和不愉悦度上均无显著差异。这一结果表明,单次α-tACS干预并未在整体行为层面上产生直接、明显的镇痛或致敏效应。
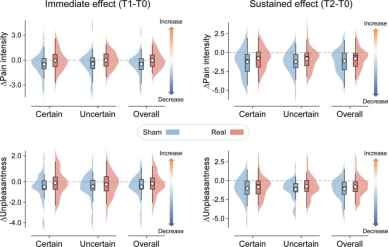
图2 α-tACS对主观疼痛评分的影响
2. α-tACS阻断了大脑对疼痛的“脱敏”(习惯化)反应
神经层面分析揭示了显著的变化。在对照组(假刺激)中,随着疼痛刺激的重复,诱发脑电N2-P2复合波的波幅出现了典型的下降(即习惯化)。然而,α-tACS削弱了大脑对疼痛的习惯化反应,尤其在确定性预期情境下。在刺激后立即(T1)和刺激后30分钟(T2)的测试中,真刺激组的N2和P2波幅均未出现类似假刺激组的大幅下降。值得注意的是,这种阻断效应具有情境依赖性:它在“确定性”疼痛预期情境下表现得最为突出且持久。
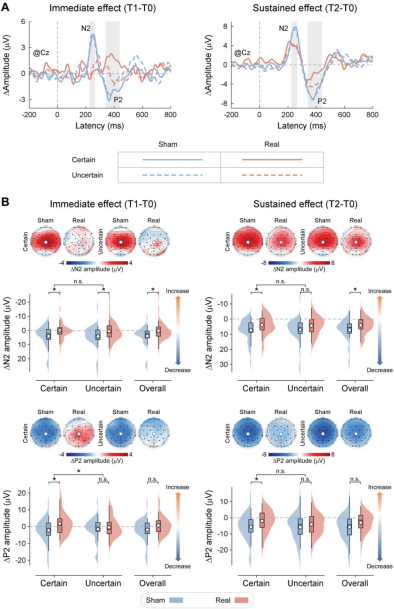
图3 感觉运动区α-tACS对激光诱发反应的影响
3. α-tACS同步增强疼痛预期阶段的两种关键脑振荡(α与θ)
在疼痛即将来临的预期阶段,对脑电振荡的分析揭示了真α-tACS带来的显著即时与持续效应,且这种效应同样高度依赖于预期情境:
感觉运动区α1振荡(8-10 Hz): 在刺激结束后立即(T1),当被试明确知道疼痛即将发生(确定性情境)时,真刺激组对侧(右侧)感觉运动区的α1振荡功率得到显著增强。但在刺激后30分钟(T2)或不确定情境下,该效应不再显著。
中额叶θ振荡(4-8 Hz): 同样在确定性情境下,真刺激显著增强了中额叶区域的θ振荡功率。与α1振荡不同的是,这种针对中额叶θ振荡的增强效应具有更强的持续性,在刺激结束后30分钟(T2)依然显著存在。
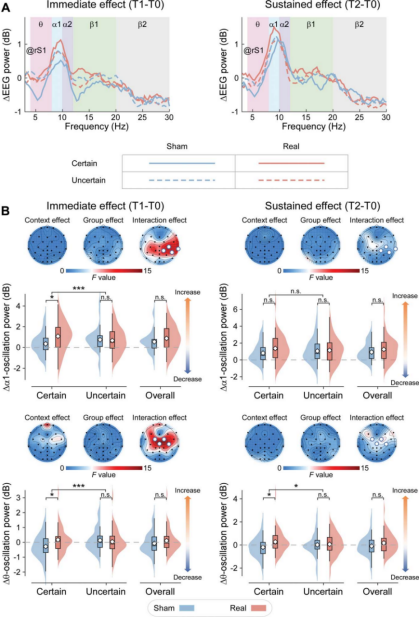
图4 感觉运动区α-tACS对预期性脑电振荡的影响
4. 中介分析揭示α与θ振荡的双重、对立调控通路
为了厘清上述神经振荡变化是如何最终影响疼痛感知的,研究者构建了中介效应模型。结果揭示,真α-tACS在脑内同时激活了两条功能完全对立的通路:
“镇痛”通路:α-tACS增强感觉运动区α1振荡,抑制了诱发脑电反应(N2-P2复合波),进而间接降低疼痛感知。
“致敏”通路:同时,α-tACS增强中额叶θ振荡,阻断了神经对疼痛反应的习惯化,进而间接增加疼痛感知。
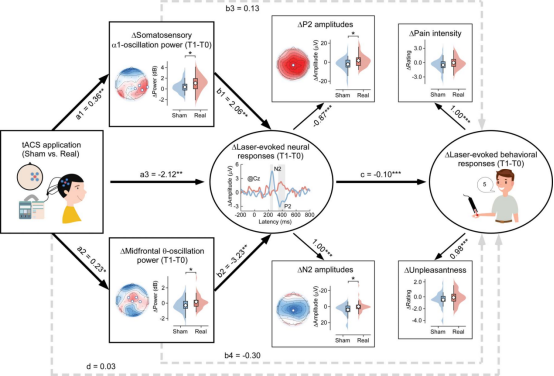
图5 躯体感觉α1振荡与额中θ振荡对疼痛的中介作用
特别值得注意的是,路径差异检验表明,由θ振荡介导的“致敏”路径在效应强度上显著大于由α1振荡介导的“镇痛”路径。这一大脑内部的“拔河比赛”完美解释了为何在整体行为层面上未观察到显著的净镇痛效果:因为较强的致敏通路在很大程度上抵消了镇痛通路的收益。
5. 效应边界:情境依赖性与时间动态性
综合上述结果,α-tACS对疼痛预期和感知的调控呈现清晰的边界条件:(1)情境依赖性:无论是感觉运动α1振荡的增强、中额叶θ振荡的增强,还是LEP习惯化的阻断,均优先或仅在确定性预期情境下显著;(2)时间动态性:感觉运动α1振荡的增强仅限于即时效应,而中额叶θ振荡的增强及LEP习惯化的阻断可持续至刺激后30分钟。
结论和意义
本研究表明,感觉运动α-tACS对疼痛的调控具有双重神经机制:一方面通过增强感觉运动α1振荡发挥镇痛作用,另一方面通过增强中额叶θ振荡产生致敏相关效应,且后者更为持久。这种对立调控的净结果受情境因素调节——在确定性预期情境下,神经层面表现为θ相关通路的激活更为显著,可能抵消了α1增强带来的潜在镇痛收益。
从临床转化角度,本研究提示未来的神经调控策略应考虑双重振荡的协同调控,例如在增强感觉运动α的同时抑制中额叶θ,或根据预期确定性的时间窗口(如手术前、分娩镇痛前)优化刺激时机。此外,本研究证实了疼痛预期阶段作为干预靶点的可行性,为通过调控预期过程改善疼痛体验提供了新的思路。
DOI:10.1097/j.pain.0000000000003452
引用:Li, X., Jin, R., Lu, X., Zhan, Y., Jiang, N., & Peng, W. (2025). Alpha transcranial alternating current stimulation modulates pain anticipation and perception in a context-dependent manner. PAIN, 166(5), 1157-1166.




